Die vorliegende Website enthält Prozentangaben, die exakt aus den entsprechenden Publikationen zitiert wurden und nicht gerundet wurden.
Viele Frauen, die Brustkrebs im Frühstadium haben, sind sich nicht bewusst, dass sie ein Risiko für späte Fernrezidive haben. Dies kann zu Unsicherheit und einer geringeren Therapietreue führen. Als Experten in der Krebsbehandlung möchten wir Ihnen hier hilfreiche Fakten und Informationen zur Verfügung stellen, damit Sie Ihre Patientinnen bei dieser Herausforderung unterstützen können.
Ein Fall aus der Praxis
- 60-jährige Frau, guter Allgemeinzustand, keine Vorerkrankungen
- Tastbarer Knoten in der linken Brust im oberen äußeren Quadranten
- Bildgebung: 2,5 cm großer Herd im oberen äußeren Quadranten der linken Brust sowie ein 1,1 cm großer suspekter axillärer Lymphknoten
- HR+/HER2- (Östrogenrezeptor-positiv > 90 %, Progesteronrezeptor-positiv > 90 %, HER2-negativ)
- Kein Hinweis auf Fernmetastasen in der Bildgebung
- Lumpektomie links und Sentinel-Lymphknotenbiopsie (SNB) und Pathologie: Unifokales invasives duktales Karzinom, 2,7 cm, 1 von 2 Sentinel-Lymphknoten war positiv (1/2 snLK)
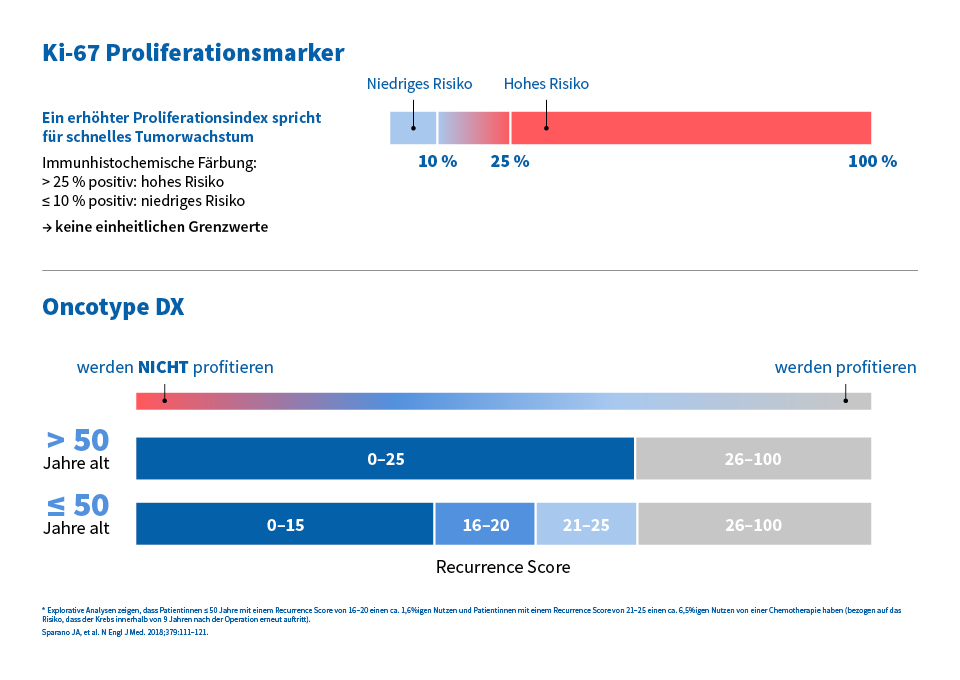
- G2; Ki-67: 26 %
- Oncotype DX Recurrence Score: 29
- Klassifikation: Stage IIB, pT2 N1 M0
Wie würden Sie das Rückfallrisiko für diese Patientin einschätzen?
Es gibt eine Tendenz, das Risiko auf ein Fernrezidiv bei Hormonrezeptor-positivem (HR+) Brustkrebs im frühen Stadium zu unterschätzen. Daher ist es wichtig zu wissen, dass der Anteil der Patientinnen mit einer Erkrankung im Stadium II (N0, N1) sowie deren Rückfallrisiko oft höher sind als angenommen.1-3
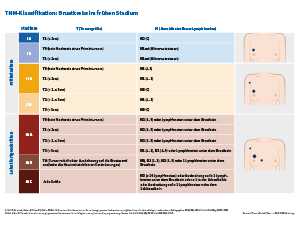
Stage II TNM-Klassifikation
Die Einteilung der Tumorstadien erfolgt nach Tumorgröße (T), Lymphknotenbeteiligung (N) und Metastasen (M) gemäß dem American Joint Committee on Cancer (AJCC).4,5
Einfach zu merken4:
- Im Stadium IIA sind alle Tumoren kleiner 2cm und 1-3 befallenen Lymphknoten oder Tumoren zwischen 2-5cm ohne Lymphknotenbeteiligung.
- Im Stadium IIB sind alle Tumoren zwischen 2-5cm mit 1-3 befallenen Lymphknoten oder Tumoren größer 5cm ohne Lymphknotenbeteiligung.

Bei etwa 1 von 3 Patientinnen mit HR+ Brustkrebs im Frühstadium II mit oder ohne Lymphknotenbeteiligung (N0, N1) kommt es innerhalb von 20 Jahren nach der Diagnose zu einem Fernrezidiv2
Ein großer Teil der Patientinnen:3


Obwohl es sich um eine heterogene Population handelt, besteht bei allen Patientinnen mit HR+ Brustkrebs im Stadium II (N0, N1) das Risiko eines Fernrezidives – selbst bei Patientinnen, die sich in einem sehr frühen Stadium mit niedriger TNM-Tumorklassifikation befinden.1
Das Risiko für ein Fernrezidiv erreicht in den ersten 3 Jahren nach der Diagnose seinen Höhepunkt.6
Mögliches Auftreten von Metastasen bei Brustkrebs im Verlauf:7
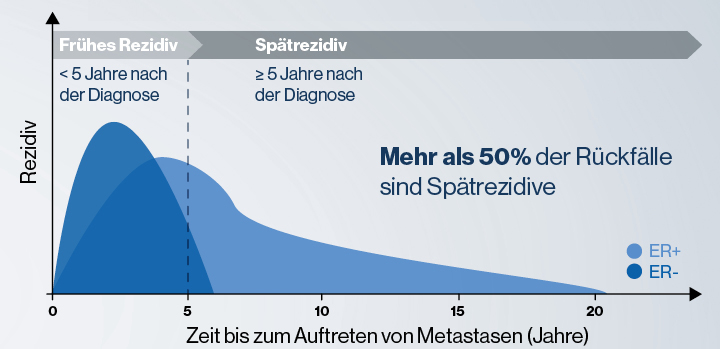
Die gestrichelte Linie zeigt die klinische Schwelle zwischen einem frühen oder späten Rezidiv an.
Anteil der Patientinnen mit Stadium II und einem Fernrezidiv über die Zeit2
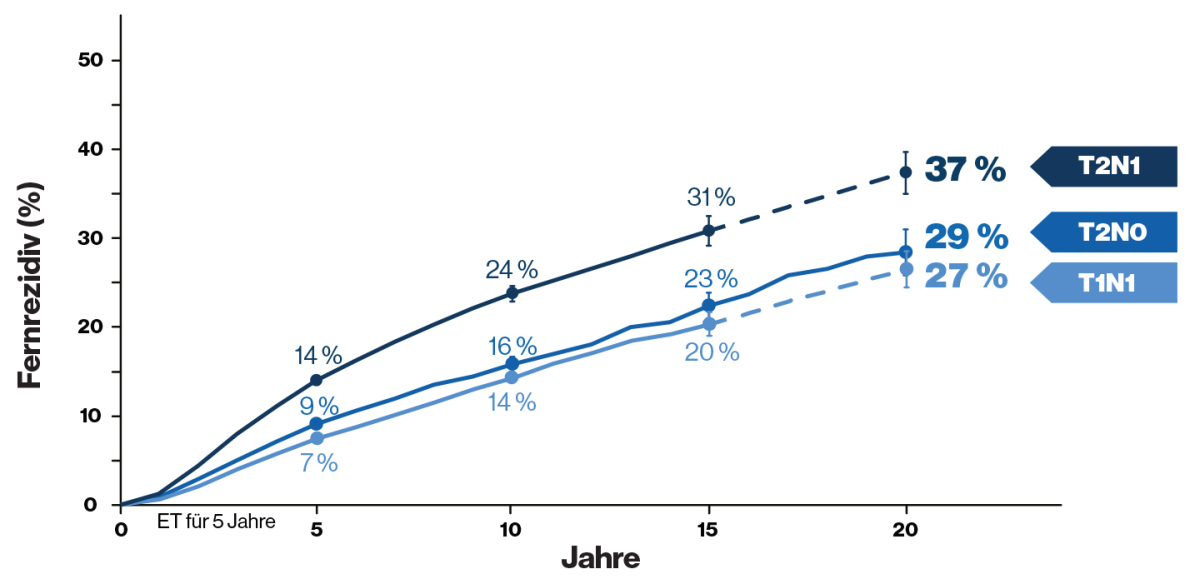

Dargestellt ist der prozentuale Anteil der Patientinnen mit Fernrezidiv über die Zeit.
Die Daten stammen aus einer Meta-Analyse* von 78 randomisierten Studien in der Datenbank der Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Darin eingeschlossen sind 74.194 Frauen mit HR+ Brustkrebs, die 5 Jahre lang eine geplante endokrine Therapie erhalten hatten. Patientinnen mit T0 und T3 sowie Patientinnen mit N3-Erkrankungen wurden nicht in die Analyse mit einbezogen.1
Die dargestellte Studie zeigt, dass 24% der Patientinnen im T2N1 Stadium (wie im obigen Patientenbeispiel) innerhalb 10 Jahren ein Fernrezidiv erleiden. Ein anderes Modell berechnet % von überlebenden Patientinnen unter Berücksichtigung verschiedener Aspekte wie Tumorgröße, Lymphknotenbefall und Tumormarker (https://breast.predict.nhs.uk/tool). Als Grundlage für die Berechnung dienen hier Daten aus wissenschaftlichen Studien, die die Wirksamkeit von Brustkrebsbehandlungen untersucht haben. Durch die Analyse der Ergebnisse dieser Studien kann das Tool berechnen, wie sich diese Aspekte wahrscheinlich auf die durchschnittliche Überlebenszeit auswirken und wie groß der durchschnittliche Nutzen der verschiedenen Behandlungsoptionen sein könnte. Da diese Berechnungen auf Daten aus Studien an ähnlichen Patientinnengruppen basieren sind sie mit Unsicherheiten behaftet und können selbstverständlich nur Schätzungen liefern.
Mangelnde Adhärenz bei der endokrinen Therapie kann für Patientinnen mit frühem Brustkrebs Folgen haben. Wenn Patientinnen ihre Medikamente nicht wie verschrieben einnehmen, kann dies zu erhöhtem Risiko für Fernmetastasen, für ein Lokalrezidiv, zu vermindertem krankheitsfreiem Überleben und erhöhtem Sterblichkeitsrisiko führen.8 Umso wichtiger ist es, gemeinsam mit den Patientinnen Lösungen zu erarbeiten, um die Einhaltung der Therapie zu erleichtern und somit die Erfolgschancen der Behandlung zu erhöhen.
In einer umfangreichen Analyse von 20.998 Patientinnen wurden die Behandlungsverläufe anhand von Daten der deutschen Krankenkasse AOK untersucht. Dabei lag der Fokus auf der Therapietreue, die durch das Verhältnis von verschriebenen Rezepten zur Therapiedauer gemessen wurde.9
Definition der Therapietreue:
(Verhältnis verschriebene Rezepte zu Therapiedauer)
- Hohe Therapietreue: Verhältnis von 0,8 bis 1,0.
- Niedrige Therapietreue: Verhältnis von 0 bis 0,8.
Unter den 17.006 HR+ eBC-Patientinnen zeigte sich, dass 49 % eine konstant hohe Therapietreue aufwiesen, während 10 % über die gesamten 5 Jahre hinweg eine niedrige Therapietreue hatten. Die konstante Einhaltung der Behandlung beeinflusste sowohl Überleben ohne Fernrezidiv (DRFS) als auch das Gesamtüberleben (OS) signifikant: Die Hazard Ratio (HR) für das DRFS lag bei 0,61 (95 %-KI: 0,52–0,71; p < 0,0001) und die HR für das OS bei 0,52 (95 %-KI: 0,46–0,59; p < 0,0001).9
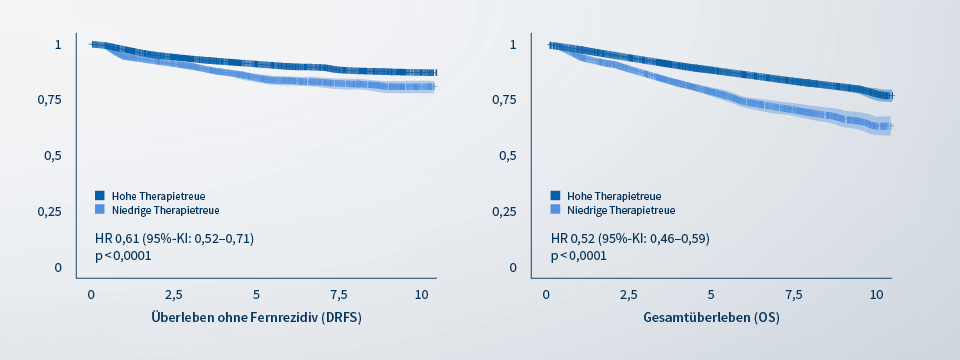
Diese Werte verdeutlichen, dass eine konstante Adhärenz mit einem geringeren Risiko einhergeht.
Die 10-Jahres-Überlebensrate lag bei Patientinnen mit hoher Therapietreue bei 79 % im Vergleich zu 64 % bei niedriger Therapietreue zur endokrinen Therapie.9
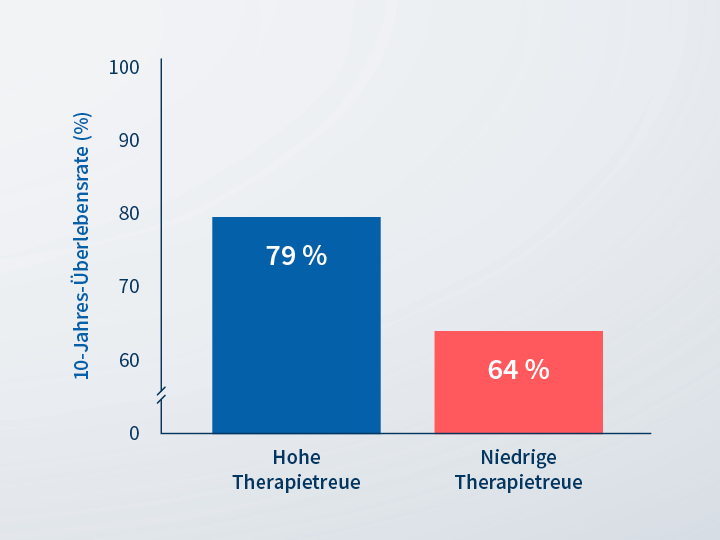
Diese Ergebnisse unterstreichen die Bedeutung der konsequenten Einhaltung der Behandlung für das langfristige Überleben.
Eine gute Kommunikation zwischen Ärzt*in und Patientin kann den Erfolg der Behandlung entscheidend verbessern. Dabei ist es wichtig, dass Patientinnen über ihr Rezidivrisiko informiert werden, ohne dabei unnötige Ängste zu schüren. Studien zeigen, dass Patientinnen, die sich ihres Risikos bewusst sind, eine höhere Therapieadhärenz aufweisen und somit bessere Heilungschancen haben. Um Sie bei der Kommunikation mit Ihren Patientinnen zu unterstützen, haben wir wertvolle Materialien rund um das Thema Rezidivrisiko zusammengestellt.
Tabellarische Übersicht zur Einordnung der TNM-Klassifikation mit ihren Patientinnen:
TNM-Klassifikation Brustkrebs im frühen Stadium
1. Kalli S, et al. American Joint Committee on Cancer’s staging system for breast cancer, eighth edition: what the radiologist needs to know. Radiographics. 2018;38(7): 1921-33. doi:10.1148/rg.2018180056 2. Koh J & Kim MJ. Introduction of a new staging system of breast cancer for radiologists: an emphasis on the prognostic stage. Korean J Radiol. 2019;20(1): 69-82. doi:10.3348/kjr.2018. 3. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®. Breast Cancer. Version 3.2023; 03/03/23.
Übersicht Ki-67 Proliferationsmarker und Oncotype DX Recurrence Score
Mögliches Auftreten von Metastasen bei Brustkrebs im Verlauf
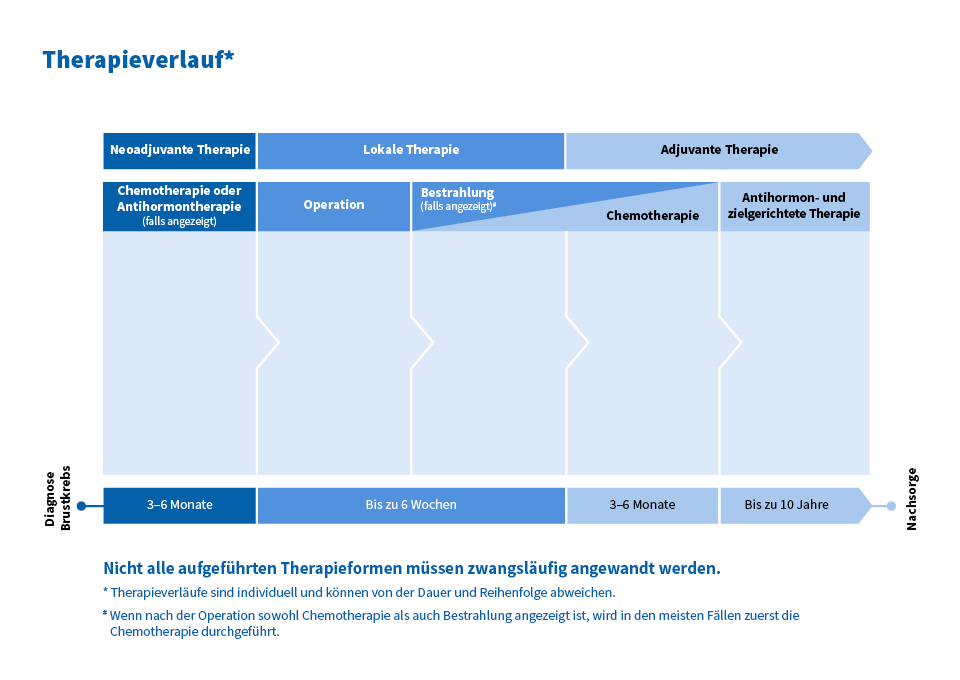
Therapieverlauf – Schema
*Meta-Analyse: Statistisches Verfahren, um die Ergebnisse verschiedener Studien, welche dieselbe Fragestellung in einem wissenschaftlichen Forschungsgebiet verfolgen, quantitativ zusammenzufassen und zu bewerten. Sie können jedoch nicht als gleichwertiger Ersatz für klinische Studien angesehen werden, mit welchen unterschiedliche Behandlungsoptionen untersucht werden.
Referenzen
- Pan H, Gray R, Braybrooke J, et al. EBCTCG. 20-year risks of breast-cancer recurrence after stopping endocrine therapy at 5 years. N Engl J Med. 2017;377(19): 1836-1846. doi:10.1056/NEJMoa1701830
- Pan H, Gray R, Braybrooke J, et al. EBCTCG. 20-year risks of breast-cancer recurrence after stopping endocrine therapy at 5 years. N Engl J Med. 2017;377(19): 1836-1846;(suppl). doi:10.1056/NEJMoa1701830
- Krebs in Deutschland für 2019/2020. 14. Ausgabe. Robert Koch-Institut (Hrsg) und die Gesellschaft der epidemiologischen Krebsregister in Deutschland e.V. (Hrsg). Berlin, 2023. Online verfügbar unter: www.krebsdaten.de. Letzter Zugriff: 24.04.2023.
- Kalli S, Semine A, Cohen S, Naber SP, Makim SS, Bahl M. American Joint Committee on Cancer’s staging system for breast cancer, eighth edition: what the radiologist needs to know. Radiographics. 2018;38(7): 1921-33. doi:10.1148/rg.2018180056
- Koh J, Kim MJ. Introduction of a new staging system of breast cancer for radiologists: an emphasis on the prognostic stage. Korean J Radiol. 2019;20(1): 69-82. doi:10.3348/kjr.2018.0231
- Bria E, Carlini P, Cuppone F, et al. Early recurrence risk: aromatase inhibitors versus tamoxifen. Expert Rev Anticancer Ther. 2010; 10(8): 1239–1253.
- Gomis RR, Gawrzak S. Tumor cell dormancy. Mol Oncol. 2017; 11(1):62–78.
- Inotai A, Ágh T, Maris R, et al. Systematic review of real-world studies evaluating the impact of medication non-adherence to endocrine therapies on hard clinical endpoints in patients with non-metastatic breast cancer. Cancer Treat Rev. 2021;100: 102264. doi: 10.1016/j.ctrv.2021.102264.
- Dannehl T, Engler T, Dijkstra T, et al. Influence of adherence to adjuvant endocrine therapy in early breast cancer: Results from a large German real-world claims data analysis. ASCO 2023. Abs. 551.